|
2019AP报考工具箱
|
||||
5.“反应级数有什么用?”
化学反应中某物质的反应级数(ReactionOrder)表示该物质浓度变化对于化学反应速率的影响,反应级数越大,表示反应速率随着浓度的变化越显著。
我们可以结合实验测定的数据将反应速率以反应物浓度及其级数表示出来。需要注意的是反应级数与化学反应配平方程式中的系数不一定一致,只有基元反应(ElementaryReaction)中配平方程式中的系数决定反应级数。
AP化学考试热门考点反应速率方程(Rate Law)与反应机理(Reaction Mechanism)需要考生深入理解反应级数对于化学反应速率的影响。
6.“Ksp是什么意思?它与Solubility有什么关系?”
Ksp是难溶盐的溶度积常数,或者称为电离平衡常数。例如对于难溶盐AgCl来说,Ksp=[Ag+][Cl-]。通常对于一种特定的难溶盐来讲,如果Ksp的数值越小,代表这种盐电离产生的离子浓度越低,也就是溶质的溶解度(MolarSolubility)越小。
AP化学考试热门考点化学平衡通常会考查不同条件下的平衡常数表达式,考生需要区分清楚每种平衡常数代表的含义。
7.什么样的反应是
thermodynamicallyfavorable?”
Thermodynamicallyfavorability描述一个反应的自发性。如果一个化学反应是自发的,也就是说它是热力学上倾向发生的反应;反之,如果一个化学反应是非自发的,也就是说它是热力学上倾向不发生的反应。我们还需要结合ΔG来进行判断。
AP化学考试热门考点吉布斯自由能(GibbsFreeEnergy)通常与焓变(EnthalpyChange)、熵变(EntropyChange),或者与平衡常数(Keq)和电池电势差(CellPotential)联系起来考查。
8.“BufferSolution为什么可以缓冲pH变化?”
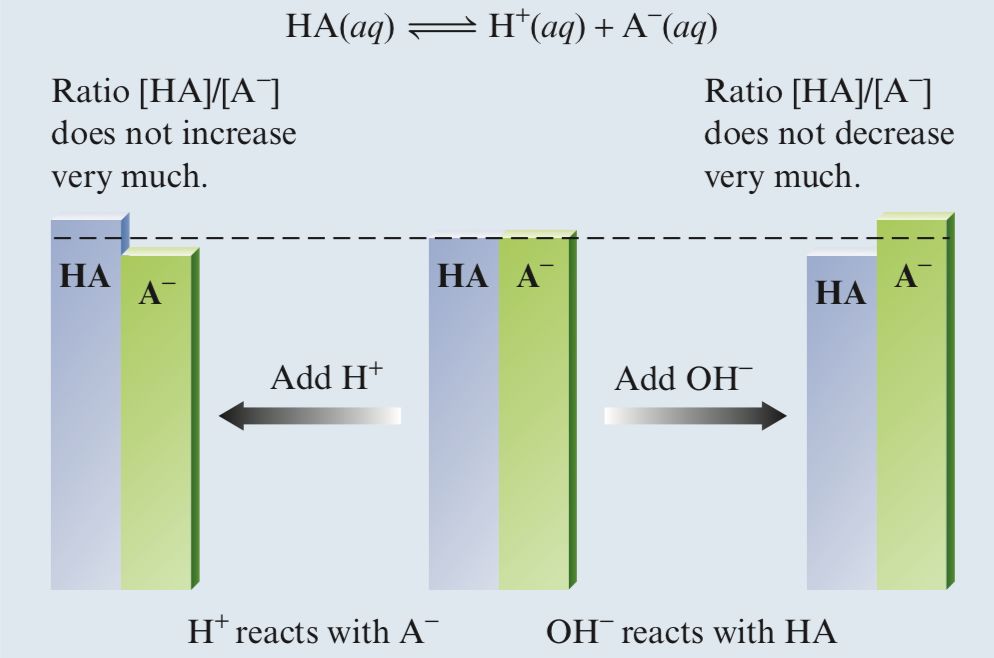
缓冲液(BufferSolution)可以延缓外加少量酸碱对溶液pH的变化,通常是由弱酸及其盐或者弱碱及其盐来构成的。
例如HA代表一种弱酸,相同浓度的HA和NaA可以构成缓冲液,如果向该溶液中加入少量的酸,溶液中的A-会与H+反应,因此加入的H+被消耗掉,缓冲液的pH不会明显降低;如果向该溶液中加入少量的碱,溶液中的HA会与OH-反应,因此加入的OH-被消耗掉,缓冲液的pH不会明显升高。
AP化学考试热门版块酸碱部分考点较多,而缓冲溶液的构成、作用与pH计算都是高频考点。